2018年全球生物藥市場達到2483億美元,復合增長率約為7.9%。在全球生物制品市場中,單抗藥物市場達到1232億美元,占比達到48%,復合增長率為14.9%,成為生物制品中占比最高的子領域。疫苗市場為305億美元,復合增長率為8.2%。全球已有近100個抗體藥物上市,主要治療腫瘤、自身免疫病等免疫相關疾病。我國抗體藥市場約為160億元左右,并以20%左右增速保持快速增長,我國單抗藥物市場份額僅占1%。遠低于歐美。
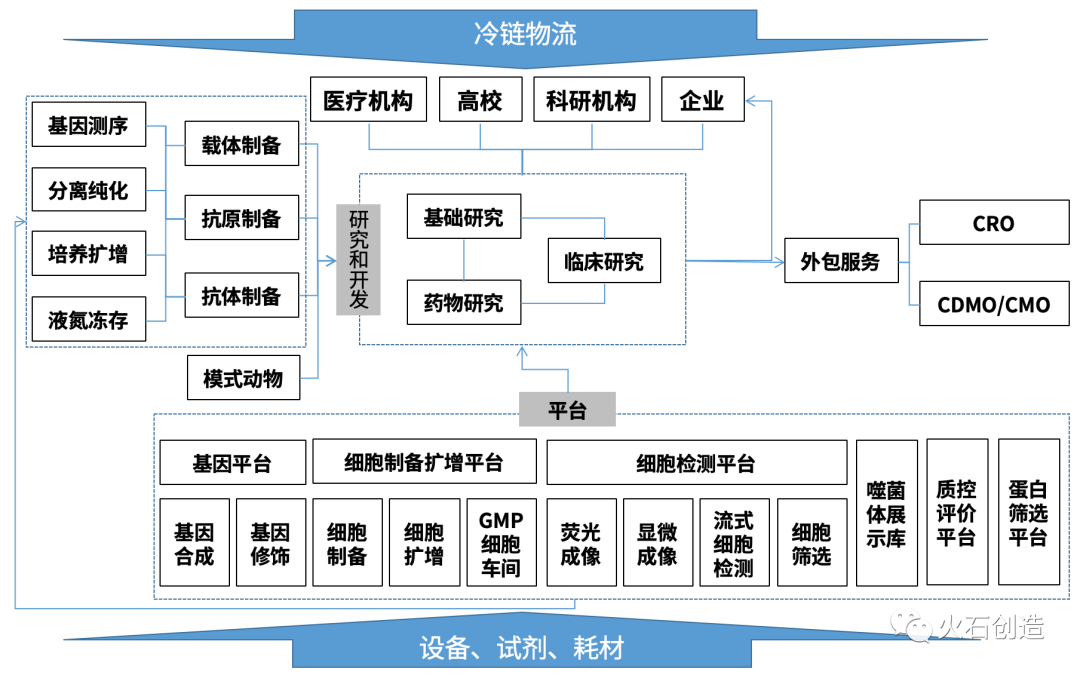
上游基礎研發是行業發展驅動力。通過廣泛深入的研究疾病發生的信號通路,發掘與疾病發生相關的基因位點與蛋白因子及其調控機理,為生物藥物的開發尋找新靶點、新方向。中游藥物研發和中試是產業核心環節。生物藥物的發現、臨床前研究與生產工藝摸索是大多數生物技術制藥企業的核心技術,相關技術平臺的建設對生物藥物的研發起著重要作用,是獲得相關技術和獨特優勢的關鍵。下游生產是實現產業化的關鍵。隨著抗體藥市場規模快速拓展,大量抗體項目從研發階段轉入生產階段,產業化體量迅速增長,多家生物制藥企業和CMO已安裝大容量生物反應器,生產技術人員需求巨增。
我國單抗藥物市場份額僅占1%。遠低于歐美,發展空間巨大。我國抗體藥物在自身免疫病、眼部疾病和心血管領域的應用遠遠低于歐美水平,隨著醫療和消費水平的快速發展,國內抗體藥物市場有巨大的增長空間。免疫治療快速發展,PD-1抗體引領免疫檢查點療法熱潮。免疫療法在腫瘤治療領域取得巨大成功,推動了免疫療法與化學藥、溶瘤病毒和CAR-T細胞治療等療法的聯用研究,全球涉及PD-1/PD-L1抗體藥物的臨床試驗已超過3000個。繼CTLA-4和PD-1/PD-L1之后,TIM-3、LAG-3、TIGIT、OX40、GITR和VISTA等免疫檢查點被相繼發掘,并開展大量臨床研究。疫情加速抗病毒藥物和疫苗研發。疫情爆發以來,生物制藥企業迅速投入抗病毒藥物和疫苗的研發,至5月底,全球已有318款治療藥物與115款疫苗在研。托珠單抗等抗體藥物已進入III期臨床試驗,重組疫苗和mRNA疫苗等進入臨床II期。靶點集中,新靶點開發風險較大。全球獲批的抗體藥靶點不到30個,約80%的在研藥物都集中在幾個常見靶點,同質化嚴重。新靶點未經驗證,具有相當高的風險。
全人源抗體、雙特異抗體、抗體藥物耦聯、納米抗體和mRNA疫苗等新技術快速發展,大量新技術藥物進入臨床試驗階段。全人源抗體的氨基酸序列全部來源于人體天然抗體序列,可有效降低免疫原性,可通過噬菌體展示、酵母展示、轉基因小鼠或單個B細胞等方式制備。目前銷售量最高的抗體藥修美樂(阿達木單抗)是全人源抗體。全人源抗體仍然不能完全避免免疫原性,具體候選分子的免疫原性仍需要分析評價。抗體偶聯藥物(ADC)將小分子藥物與抗體偶聯,既有抗體對靶點的特異性識別,也能夠通過小分子藥物高效清除癌細胞,有效降低系統性化療帶來的副作用。小分子藥物通過化學鍵構成的接頭連接在抗體上,接頭按其穩定性分為不穩定接頭和可切斷接頭,配合不同的靶點-抗體組合,可以實現不同的治療策略,如通過不穩定接頭和低毒性小分子配合,利用旁觀者效應殺傷腫瘤。全球有7個ADC藥物上市,國內百奧泰、榮昌生物、四川科倫、蘇州東曜和江蘇恒瑞等企業有ADC產品開展臨床試驗。雙特異抗體是含有兩個特異性抗原結合位點的人工抗體,可以同時結合兩個不同的特異性表位。通過同時識別兩個標靶,雙特異性抗體可以作為一個媒介雙重定向免疫效應細胞,將效應細胞直接靶向腫瘤細胞,增強對腫瘤的殺傷力,通過協同效應起到“1+1>2”的治療功效。全球目前有2個雙特異抗體藥物上市,安進、羅氏、艾伯維和強生等制藥巨頭布局雙特異抗體研發。國內友芝友生物、中山康方和岸邁生物等企業有雙特異抗體進入監試研究階段。納米抗體是抗體片段的一種,是駱駝和鯊魚體內的天然抗體,其相對分子質量較小,具有較強的組織穿透力、親和力高、免疫原性較小、易于生產等優勢。Ablynx是全球納米抗體藥物的領軍者,已有8個納米抗體進入臨床研究階段。國內有蘇州康寧杰瑞、博生吉和深圳普瑞金等公司開發納米抗體藥物。mRNA可以快速地在細胞內翻譯,表達所需蛋白,適用于制作抗感染疫苗和腫瘤疫苗。然而,mRNA非常不穩定,需要先進的序列修飾和制劑技術保護mRNA。全球研發mRNA藥物的知名公司有BioNTech、Moderna和CureVac等,都通過納米脂質體技術保護mRNA。新冠肺炎疫情爆發以來,Moderna、斯微生物和中國人民解放軍軍事科學院軍事醫學研究院等企業及機構緊急攻關,多個針對新冠病毒的mRNA疫苗已進入臨床研究階段。
(作者:楊周寧)
化學藥產業是我國生物醫藥產業的重要組成部分,估計2019年,中國化學藥市場規模將突破8000億元。總體來說,國內化藥原料藥、中間體產業相對成熟,在全球產業鏈上地位較高;化學制劑與領先國家存在差距,仿制藥大而不強,創新藥剛起步。
中國一直在由傳統化學原料藥、仿制藥向創新藥研發的道路上前進,近年來,一致性評價、帶量采購、MAH制度等政策的出臺極大地改善了中國化學藥的發展環境,一方面加劇了市場競爭,另一方面,也規范了市場,提高了藥品的質量,使得優質企業擁有更好的發展機遇。未來,國內化學藥制劑產業將繼續在政策以及市場的導向下加大創新投入,加速升級轉型。1.化學新藥政策環境得以根本改善,鼓勵政策貫穿臨床研發、審評審批、生產制造、醫保支付等藥品全生命周期。2015年國務院印發《關于改革藥品醫療器械審評審批制度的意見》(國發〔2015〕44號),由此此拉開了我國新藥鼓勵政策的序幕。2019年12月1日新修訂的《中華人民共和國藥品管理法》正式施行,將我國新時期新藥鼓勵政策實踐成果以法律的形式得以確定。我國新藥政策改革以審評審批制度為突破口,逐漸覆蓋至臨床試驗管理、知識產權保護、藥品上市許可持有人制度(MAH)試點、創新藥入醫保藥品目錄等多個產業環節,由此,我國新藥創制的政策環境得以根本改善。圖1 “十三五”期間我國鼓勵新藥創制政策“里程碑”2. 鼓勵仿制藥目錄政策出臺,一致性評價、帶量采購改變國內仿制藥市場格局。2019年10月9日,國家衛健委印發《關于印發第一批鼓勵仿制藥品目錄的通知》,目錄包括了抗癌藥、罕見病用藥及免疫系統治療藥物等33種藥品,主要為國內專利到期和專利即將到期尚沒有提出注冊申請、臨床供應短缺、市場競爭競爭不充分的藥品,如遺傳病藥尼替西農、HIV藥物阿巴卡韋、抗腫瘤藥物甲氨嘌呤等。該政策出臺后,各大知名藥企紛紛響應,積極布局高端仿制藥及首仿管線,放棄低端仿制藥研發生產,加速了企業的升級轉型。此外,在學習先進國家醫藥市場改革經驗的基礎上,國家陸續推出一致性評價、帶量采購等重磅改革政策,為全面提高化學仿制藥質量,節約醫保開支,保障用藥安全作出了突出貢獻。當下,國內正處于高仿、首仿政策利好時期,在政策鼓勵下,高質量的優質仿制藥快速獲批上市,而低端仿制藥則面臨質量嚴控、“以價換量,以量換價”的現狀。仿制藥行業政策有利于促進行業有序發展,未來仿制藥企業競爭將會日益加劇,行業集中度上升,市場格局將繼續發生重大變化。3.多款重磅化學制劑新藥獲批上市,化學新藥藥品治療領域集中在抗腫瘤、HIV、丙肝、2型糖尿病以及罕見性疾病等領域。在抗腫瘤藥物方面,涌現出針對晚期或轉移性非小細胞肺癌及軟組織肉瘤的多靶點酪氨酸激酶抑制劑藥物鹽酸安羅替尼、治療復發或轉移性乳腺癌的口服的表皮生長因子受體(EGFR)和HER2酪氨酸激酶的雙重抑制劑藥物馬來酸吡咯替尼以及針對轉移性結直腸癌的新型高選擇性血管內皮細胞生長因子受體(VEGFR)抑制劑藥物呋喹替尼。安羅替尼是我國第一個軟組織肉瘤靶向藥,獲得美國FDA授予軟組織肉瘤孤兒藥的資格。安羅替尼2018年獲批上市以后,接近半年銷售額就達到12.8億元,2019年全年銷售額估計高達30億元。在病毒性肝炎、艾滋病、流感等重大病毒性感染疾病相關治療藥物方面,艾博韋泰是國內首個、全球第二個抗艾滋病長效藥物,對主要流行的HIV-1病毒及耐藥病毒均有效,具有安全性高、副作用小等優勢。達諾瑞韋鈉是中國首個本土研制口服治療慢性丙型肝炎的1類新藥,是具有新作用機制的特異性靶向的抗丙型肝炎病毒的藥物。此外,1類新藥可利霉素是針對耐藥的革蘭氏陽性菌、肺炎支原體、衣原體等引起的上呼吸道感染藥物,具有口服吸收度高、劑量小、不良反應發生率和誘導耐藥率低的特點。針對慢性腎性貧血藥物羅沙司他,是歷史上首個全球同步開發、中國首發的1類新藥,該藥是全球首個小分子低氧誘導因子脯氨酰羥化酶抑制劑類治療腎性貧血的藥物。針對銀屑病藥物本維莫德,是全球第一個有治療作用的芳香烴受體調節劑類、非激素小分子化學藥物,可多通路抑制銀屑病發病環節,療效確切,復發率低。表1 2016—2020年5月20日CDE批準上市的重磅化學新藥3.心腦血管、腫瘤、呼吸、糖尿病等慢性疾病將繼續成為化學藥重點研發適應癥方向。隨著工業化、城鎮化、人口老齡化進展和生態環境、生活方式變化,慢性非傳染病疾病已經成為我國居民主要死亡原因和疾病負擔,目前我國心腦血管疾病、癌癥、慢性呼吸系統疾病、糖尿病等慢性非傳染性疾病死亡人數占總死亡人數的88%,導致的疾病負擔占總疾病負擔的70%以上,是普遍影響我國居民健康的主要疾病,成為制約健康預期壽命提高的重要因素。同時,肝炎、結核病、艾滋病等重大傳染病防控形勢依然嚴峻,地方病、寄生蟲病等仍然嚴重威脅流行地區居民的健康。“聯合國2030年可持續發展議程”將降低這四類重大慢性病導致的過早死亡率作為重要的發展目標。“健康中國2030”規劃綱要也將這個目標納入健康中國建設的主要指標。因此,從臨床需求來看,未來我國的化學創新藥、高端仿制藥研發將主要集中在惡性腫瘤、心腦血管疾病、糖尿病和呼吸系統疾病等慢性病領域;在新冠病毒全球蔓延的背景下,抗感染、抗病毒藥物仍將保持一定的研發比例。4.化學藥新藥創新主體成頭部大型企業、中小型初創企業以及科研院所“三足鼎立”之勢,研發服務體系不斷完善。大型創新藥研發企業早期通過與科研院所、大學合作開發新藥,企業重視研發團隊建設,新藥研發投入大,現階段企業的創新藥管線已初具規模的代表企業有恒瑞醫藥、豪森藥業、正大天晴、石藥集團、貝達藥業、東陽光藥業等。微創型企業通過金融市場獲得資金支持,專注于某一治療領域,以抗腫瘤藥物為主,研發團隊成員具有海外科研背景或者跨國制藥企業背景,研發產品面向全球,以自主研發、引進開發 (如license-in)、合作外包等多種方式開發新藥,代表企業有蘇州澤璟生物、南京圣和藥業、廣東眾生藥業、基石藥業、和記黃埔、綠谷制藥、百濟神州、卡南吉、再鼎醫藥等。科研院所以中國科學院上海藥物研究所、中國醫學科學院藥物研究所、上海醫藥工業研究院、中國藥科大學、沈陽藥科大學、四川大學為代表,研發實力較強,通常與企業合作進行創新藥開發。5.化學制劑資本市場熱度不減,融資主要集中在創新化藥研發企業,仿制藥企業融資事件小。2019年,國內化學藥領域共發生融資事件49起,涉及44家企業,24起項目已披露融資金額,融資總金額為74.80億元。江蘇、上海、廣州融資項目數量位居前三,累計占46.9%;上海、北京、江蘇融資金額位居前三,累計占67.3%。圖3 我國部分重點省市已披露化學藥領域融資情況
數據來源:火石創造
49融資事件中,有披露的億元及以上融資事件19起,10億元及以上融資事件2起,分別是艾力斯醫藥11.8億元A輪融資和諾誠健華1.6億美元戰略融資。艾力斯醫藥聚焦抗腫瘤、抗高血壓、抗糖尿病等重大疾病,目前公司已擁有1.1類抗高血壓藥物阿利沙坦酯,研發管線聚焦抗腫瘤藥物。諾誠健華的聯合創始人之一是我國生命科學領域頂尖科學家施一公,公司致力于研發抗腫瘤及自身免疫性疾病的分子靶向藥物,已研發出九種候選化合物,目前公司已經于港股上市。從獲得融資的創新藥企研發管線中可以看出,小分子抗腫瘤化學創新藥仍是目前資本關注的焦點,心血管、糖尿病等慢病領域也成為市場青睞的熱點。而仿制藥產業已經不是資本追逐的技術風口,只有較少的優質中小型仿制藥企業依靠其科研創新能力獲得融資,如生產高端仿制藥和擁有技術瓶頸的難仿藥的南京方生和、長風藥業、博瑞醫藥等。
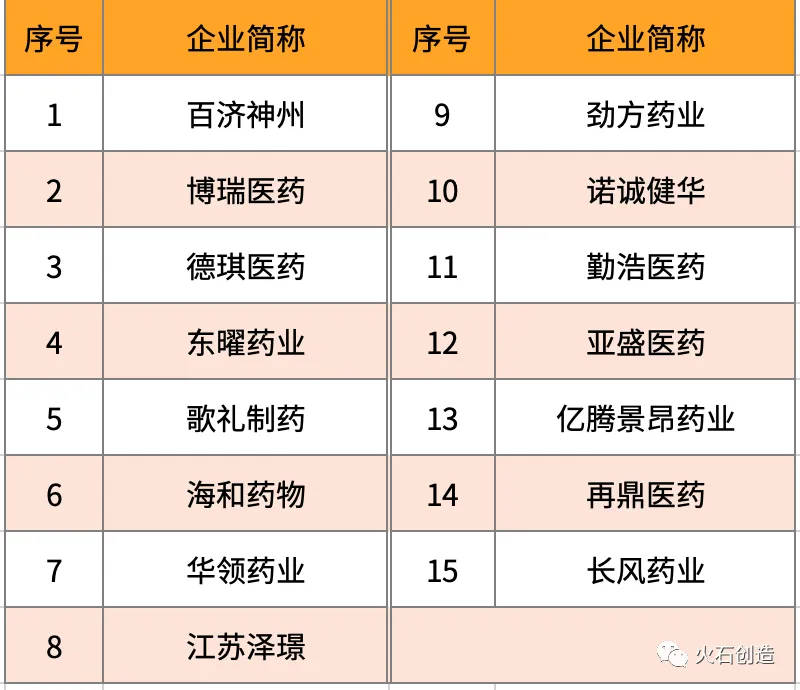
附表 我國部分化學制劑領域企業